Метаболизм аминокислот
- Определение аминокислот
- Белки
- Синтез протеиногенных аминокислот
- белка
- Транспортные белки
- Переаминирование аминокислот
- Пиридоксаль фосфат
- Дезаминирование аминокислот
- Окислительное дезаминирование
- Гидролитическое дезаминирование
- Элиминативное дезаминирование
- Декарбоксилирование аминокислот
- Центральные аминокислоты
- Глютамин, глутамат и альфа-кетоглутарат
- Аланин и пируват
- Аспартат и оксалоацетат
- Семейный серин
- Метиониновый катаболизм
- Цистеиновый обмен и здоровье
- Другие метаболизм цистеина
- Селеноцистеиновый обмен
- Семья Аспартат
- Метаболизм аспарагина
- Метиониновый обмен
- Метаболизм лизина
- Фенилаланин (PHE)
- Метаболизм и болезнь тирозина
- Семья Пируват
- Метаболизм лейцина (LEU) / валина (VAL) / изолейцина (ILE)
- Гистидин (HIS) метаболизм
- Обзорные вопросы
Образ : «Структура белка NOTCH2.» От Emw. Лицензия: CC BY-SA 3.0
Определение аминокислот
Аминокислоты являются частью строительных блоков, из которых состоят белки. Аминокислоты образуют полимеры с пептидными связями . Эти полимеры более известны как белки и представляют, наряду с углеводами и жирами, основной компонент пищи и организма. Поскольку аминокислоты, как следует из их названия, включают азотистую аминогруппу в своей базовой структуре (NH2, NH, N), белки являются важным донором азота . Азот необходим для многих соединений и функций. Вот почему белки, хотя они и являются важным компонентом питания, представляют интерес лишь для части энергии (хотя они по-прежнему обеспечивают значительную часть общего количества энергии); скорее, организм нуждается в них в качестве поставщика аминокислот. С аминокислотами, поставляемыми белками и уже присутствующими в организме, могут быть созданы новые белки .
Белки
Функции белков
Белки служат:
- Строительные материалы: например, кератин в ногтях пальцев рук и ног, ткани, мышцы, кости, кожа волос.
- Транспортные средства: например, Альбумин в кровообращении, они придают клеткам свою форму.
- Сигнальные вещества: например, белок G в сигнальной трансдукции.
- Инструменты: например, ферменты для синтеза и разрушения структур.
Белки настолько элементарны, что их руководство по конструированию кодируется в ДНК нашего генетического состава. Только с их помощью организм может быть построен функционально и оперативно, потому что необходимыми инструментами и строителями всегда являются белки. Они составляют не менее 20% человеческого организма. Аминокислоты настолько важны, что их нельзя растрачивать. Поэтому постоянные процессы разрушения и восстановления организма требуют гениальной системы рециркуляции: метаболизма аминокислот.
Синтез протеиногенных аминокислот
Существует не менее 1000 различных белков, но для человеческого организма важны, в основном, протеиногенные аминокислоты. Протеиногенные аминокислоты, содержащие от 20 до 21 аминокислоты, образуют основные модули белков. Иногда также полунезаменимая аминокислота селеноцистеин считается протеиногенной аминокислотой, которая составляет число 21. В следующей таблице приведены 20 протеиногенных аминокислот с включенными основными характеристиками:
белка
Характеристика
Лизин Положительно заряженный Аргинин Положительно заряженные аспартаты Отрицательно заряженный Глутамат Отрицательно заряженного серин полярного треонина полярного аспарагин полярного Глутамат полярного гистидин полярного тирозин полярного аланин гидрофобного валин гидрофобного лейцин изолейцин гидрофобного гидрофобный Proline гидрофобного фенилаланин гидрофобного Trytophane гидрофобного цистеин гидрофобного метионин гидрофобного глицин Не имеет боковую цепь
Подобно алфавиту, где различные комбинации букв образуют новые слова, эти 21 аминокислота могут образовывать много разных белков, которые выполняют много разных задач. Аминокислоты попадают в организм в виде белков, например, в сою, молоко или мясо.
Транспортные белки
Благодаря механизмам пищеварения, аминокислоты расщепляются и попадают в кровообращение на определенных транспортных средствах. Затем они направляются в клетки организма, опять же с помощью транспортных белков . Конкретные транспортные белки облегчают диффузию или активно транспортируют определенные вещества в организме через мембраны. Транспортные белки могут быть каналом / порой, которая делает отверстия в мембранах или носителями, которые открывают одну сторону мембраны. Метаболизация аминокислот, поступающих после приема пищи, происходит главным образом в печени и почках. Кроме того, регулярное разрушение физиологических структур (например, мышечного белка) постоянно обеспечивает запас свободных аминокислот, так что всегда присутствует постоянный пул свободных аминокислот. Для аминокислоты в пуле аминокислот есть три варианта путешествия:
- Интеграция в структурные и тканевые белки для регенерации тканевых структур
- Катаболизм: дезаминирование (удаление аминогруппы) и окисление углеродного каркаса с выделением CO2 и АТФ или преобразование в накопители энергии, такие как гликоген или липиды, и синтез мочевины из аминогруппы.
- Анаболизм: синтез азотистых соединений, таких как пуриновые основания, креатин или адреналин.
Три наиболее важные реакции в метаболизме аминокислот - это переаминирование , дезаминирование и декарбоксилирование . В зависимости от текущего состояния обмена веществ существующие аминокислоты либо перегруппируются, либо полностью расщепляются.
Переаминирование аминокислот
Одной из центральных реакций метаболизма аминокислот является трансаминирование. Как следует из названия, трансаминирование относится к переносу аминогруппы . Процесс трансаминирования происходит с помощью аминотрансферазных ферментов, которые могут быть специфичными для аминокислоты или могут обслуживать несколько аминокислот, которые схожи по своему химическому составу. В настоящее время не требуется, может быть преобразована в другую аминокислоту, которая в настоящее время необходима. Перераспределение аминогруппы происходит через альфа-кетокислоту, которая в основном имеет структуру, аналогичную альфа-аминокислотам . Альфа-кетокислоты отличаются только от альфа-аминокислот наличием кетогруппы вместо аминогруппы.
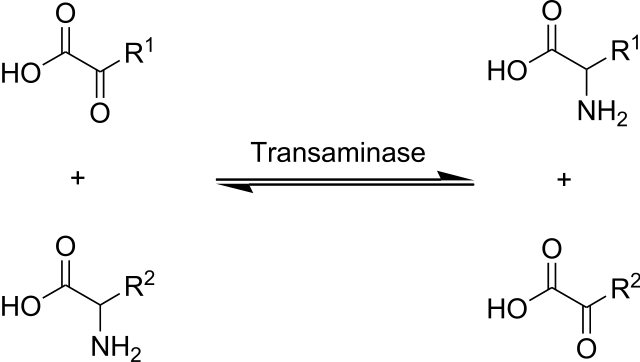
Образ : «Аминотрансферная реакция между аминокислотой и альфа-кетокислотой». Alcibiades. Лицензия: всеобщее достояние
Трансаминирование превращает альфа-кетокислоту в новую аминокислоту, доступную для обмена веществ. Ответственный фермент называется аминотрансферазой (или трансаминазой) . Аминотрансфераза, однако, нуждается в помощнике для выполнения своей работы: пиридоксальфосфат (PLP) . Это кофермент, вырабатываемый из витамина В6 (пиридоксина) путем фосфорилирования. PLP имеет альдегидную группу (HC = O), которая реагирует при переаминировании с аминогруппой аминокислоты (с удалением H2O). При этом образуется основание Шиффа (R-NH2) . Эта реакция дестабилизирует аминокислоту, и атом водорода начинает мигрировать, что, в свою очередь, приводит к сдвигу двойной связи, и кетамин (RC = O) выходит из прежнего альдимина (HC = O).
Затем через эту двойную связь добавляется вода, которая завершает образование альфа-кетокислоты. PLP восстанавливается до PMP (пиридоксаминфосфат). Обратная реакция также является распространенным вариантом получения другой аминокислоты: пиридоксаминфосфат реагирует с другой альфа-кетокислотой и PLP восстанавливается.
Двумя наиболее важными трансаминазами являются аланина трансаминаза (сокращенно ALT или ALAT ) и аспартат трансаминаза (сокращенно AST или ASAT ). ALAT катализирует перенос аминогруппы от аланина к альфа-кетоглутарату, образуя пируват и глутамат (что делает его прежним названием глутамат-пируват-трансаминаза, GPT). ASAT переводит аминогруппу из аспартата в альфа-кетоглутарат, образуя оксалоацетат и глутамат. Обе трансаминазы являются важными диагностическими маркерами: повышенные значения в общем анализе крови указывают на распад клеток в печени (ALAT) и сердце (ASAT и ALAT).
Пиридоксаль фосфат
Пиридоксальфосфат, или короткий PLP, является наиболее важным коферментом в метаболизме аминокислот. PLP является биологически активной формой пиридоксаля, альдегидной формы витамина B6. Витамин B6 также появляется в виде амина (пиридоксамин) и алкоголя (пиридоксин). Производные витамина В6 могут превращаться друг в друга. Они попадают в организм и могут содержаться в пищевых продуктах животного происхождения (пиридоксаль и пиридоксин), а также в пищевых продуктах растительного происхождения (пиридоксин).
Относительно богаты витамином В6 зародыши пшеницы. PLP в качестве кофермента участвует в метаболизме аминокислот в реакциях переаминирования, декарбоксилирования (например, образования биогенных аминов) и дезаминирования. PLP связывается с остатком лизина соответствующего фермента реакции, например, аланина трансаминазы (ALT), и создает основание Шиффа с аминокислотой. Азот PLP, содержащийся в пиримидиновом кольце, обладает сильным электрофильным эффектом, который приводит к смещению связей. В результате этой реакции образуется токсичный аммиак, концентрация которого всегда должна быть минимальной, а выбрасывать азот непригодно, поэтому происходит цикл мочевины. Приводит к дезаминированию аминокислот.
Дезаминирование аминокислот
Когда существует избыток азота в форме аминокислот, его необходимо утилизировать где-то в организме. Дезаминирование - это процесс, который осуществляет расщепление аминокислот. Однако этот процесс высвобождает свободный цитотоксический аммиак, который должен быстро метаболизироваться в мочевину. Этот синтез мочевины, который требует много энергии, происходит в печени. Для этого избыточный азот необходимо транспортировать с периферии в печень. В этом транспорте участвуют три центральные аминокислоты: аланин (синтезируется из пирувата), глутамин (синтезируется из аспартата) и аспартат (синтезируется из оксалоацетата).
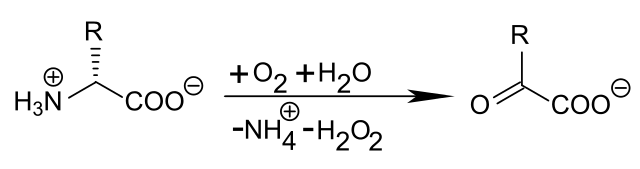
Образ : «Дезаминирование D-аминокислоты с помощью D-аминокислоты оксидазы». Куеби. Лицензия: всеобщее достояние
Дезаминирование можно разделить на три разные реакции:
- Окислительное дезаминирование
- Гидролитическое дезаминирование
- Элиминативное дезаминирование
Окислительное дезаминирование
Как и при переаминировании, основание Шиффа образуется с дегидрогеназой; более конкретно, окисление превращает аминогруппу в иминогруппу (C = N) . Акцепторами электронов являются коферменты NAD + или NADP +, которые в этом процессе восстанавливаются до NADH / H или NADPH / H соответственно. При добавлении воды иминогруппа превращается в альфа-кетогруппу, которая выделяет аммиак (NH3).
Пример : реакция глутаматдегидрогеназы с глутаматдегидрогеназой: глутамат - иминокислота - альфа-кетоглутарат. В печени глутамат из цитозоля попадает в митохондрию, где происходит окислительное дезаминирование, под воздействием фермента L-глутаматдегидрогеназы , расположенной в митохондриальном матриксе.
Гидролитическое дезаминирование
При гидролитическом дезаминировании вода реагирует с аминогруппой. Таким образом, гидроксильная группа (ОН-группа) необратимо присоединяется, и аминогруппа удаляется в форме аммиака. В реакции глутаминазы от глютамина к глутамату ответственным ферментом является глутаминаза. Та же самая реакция происходит от аспарагиновой аминокислоты до аспартата (ответственный фермент по совпадению называется аспарагиназой).
Элиминативное дезаминирование
Небольшие аминокислоты, такие как серин или цистеин, также могут высвобождаться путем элиминативного десаминирования их азота (в форме аммиака) и путем удаления воды или сероводорода для сернистых аминокислот. Для этой реакции еще раз PLP необходим в качестве партнера. Эта гидратация создает двойную связь и, после следующего гидролиза, еще одну альфа-кетокислоту.
Декарбоксилирование аминокислот
Когда карбоксильная группа отщепляется от аминокислоты, один амин и CO2 выделяются в качестве побочных продуктов. Реакция катализируется ферментом декарбоксилазой с использованием PLP в качестве партнера. Полученные амины выполняют важные функции в организме, поэтому их называют биогенными аминами .
Хорошо известным представителем является гистамин, который образуется в результате декарбоксилирования из основной аминокислоты гистидина. Ответственный фермент называется гистидиндекарбоксилазой. Гистамин является важным медиатором и играет жизненно важную роль, например, в реакциях немедленной гиперчувствительности. Другими хорошо известными биогенными аминами, релевантными для метаболизма, являются, например, ГАМК (гамма-аминомасляная кислота из глютаминовой кислоты) и дофамин (из 3,4-дигидроксифенилаланина).
Центральные аминокислоты
Есть четыре аминокислоты и их кетокислоты, которые можно описать как центральный центр метаболизма аминокислот, потому что они имеют особое значение, и наиболее важные метаболические пути проходят через эти аминокислоты:
- Глутамат и альфа-кетоглутарат
- Глютамин и альфа-кетоглутарат
- Аланин и пируват
- Аспартат и оксалоацетат
Глютамин, глутамат и альфа-кетоглутарат
Глютамин - это аминокислота, которая чаще всего встречается в плазме крови. Глютамин транспортирует азот во все клетки организма, которые в нем нуждаются, например, для синтеза пурина и пиримидина в процессе биосинтеза нуклеотидов. Глютамин также необходим в качестве донора аминокислот: он дезаминируется в почках, чтобы получить свободный аммиак.
Аммиак выделяется в проксимальных канальцах и нейтрализует кислоты в моче, образуя тем самым ионы аммония (NH4 +). В этом процессе альфа-кетоглутарат, который может быть непосредственно направлен в цикл лимонной кислоты, образуется из глютамина через глутамат. Это убивает двух зайцев одним выстрелом, поскольку альфа-кетоглутарат пополняет цикл лимонной кислоты, когда оксалоацетат выводится из него для глюконеогенеза.
Аланин и пируват
Аминокислота аланин является аналогом пирувата альфа-кетокислоты, то есть его соли (пировиноградная кислота, альфа-кетопропионовая кислота). Через пируват и аланин аминокислоты могут быть направлены в цикл лимонной кислоты и разложены на CO2 и энергию. Другой возможностью является синтез глюкозы из пирувата в глюконеогенезе или метаболизация пирувата в лактат в анаэробных условиях.
Аланин - пируват
1) СО2 + АТФ
Или 2) глюкоза
Или 3) Лактат
Когда аланин разрушается в мышцах, он сначала попадает в кровь через печень. Там происходит синтез глюкозы в глюконеогенезе на основе пирувата, полученного в результате переаминирования. Глюкоза проходит через кровоток к мышцам и обеспечивает поступление энергии в мышечные клетки путем расщепления глюкозы при гликолизе.
Это снова дает пируват. Через реакцию трансаминирования пируват получает аминогруппу аминокислоты от распада мышечного белка. Аланин поступает в печень, где его снова трансаминируют в пируват, и теперь он доступен для синтеза глюкозы в глюконеогенезе. Фермент, который отвечает за передачу аминогрупп туда и обратно, называется аланинаминотрансферазой (ALT, ALAT) .
Аспартат и оксалоацетат
Другой важной реакционной парой являются аминокислоты аспартат и оксалоацетат (альфа-кетопировиноградная кислота) . Их трансформация катализируется ферментом аспартатаминотрансферазой (AST, ASAT), концентрацию которого также можно определить в качестве диагностического маркера в анализе крови. ASAT катализирует перенос аминогруппы из аспартата в альфа-кетоглутарат с образованием оксалоацетата и глутамата. Вот почему этот фермент ранее был известен под названием глутамат оксалоацетат трансаминазы (GOT).
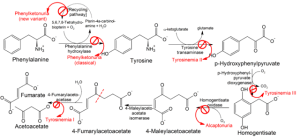
Образ : «» От LHcheM. Лицензия: CC BY-SA 3.0
Увеличение ASAT в крови может указывать на заболевания печени и сердца, потому что этот фермент присутствует в большом количестве в гепатоцитах и клетках сердечной мышцы. Таким образом, когда эти клетки разрушаются из-за патологических изменений, присутствие ASAT в крови увеличивается. Оксалоацетат может участвовать в цикле лимонной кислоты или в глюконеогенезе. Глутамат может быть далее преобразован в альфа-кетоглутарат или, например, использоваться при окислительном дезаминировании для синтеза аммиака в почках.
Семейный серин
Два основных пути ведут к серину
1. Из 3-фосфоглицерата (соединение с гликолизом)
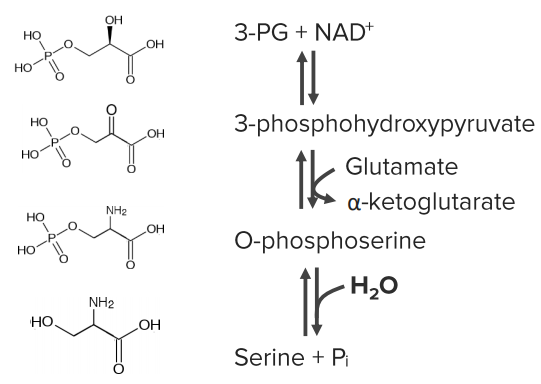
2. Обмен углерода с глицином и фолатами (важно для переработки фолиевой кислоты)
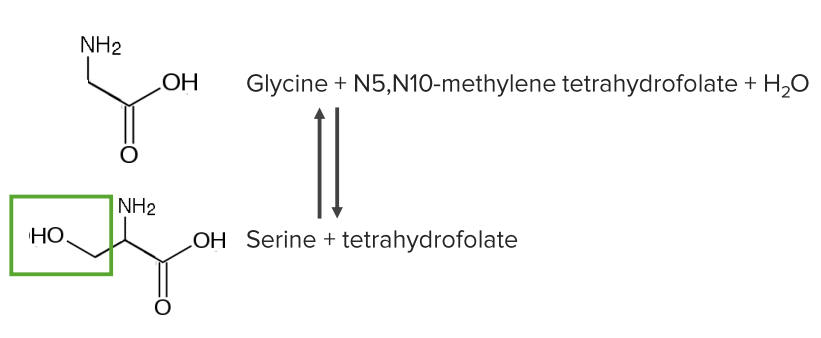
Метаболизм цистеина Множество способов получения цистеина Первичные средства, связанные с катаболизмом метионина
Метиониновый катаболизм
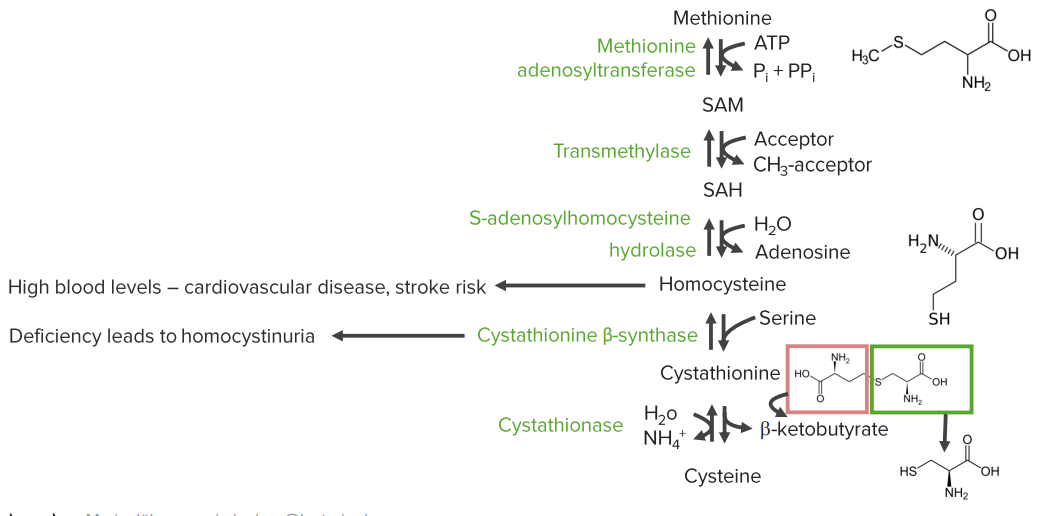
Цистеиновый обмен и здоровье
Гомоцистинурия является генетическим заболеванием. Это чаще всего включает мутацию цистатион-β-синтазы. Проблемы могут включать в себя:
- Скелетно-мышечные аномалии
- Глазные аномалии: катаракта, глаукома, отслоение сетчатки
- Ограниченными интеллектуальными возможностями
- Приступы
- Сосудистое заболевание
- Цистинурия - неродственное генетическое заболевание
- Неспособность почек реабсорбировать цистеин приводит к высокому уровню цистеина, орнитина и аргинина в моче.
- Частые почечные камни также встречаются
Другие метаболизм цистеина
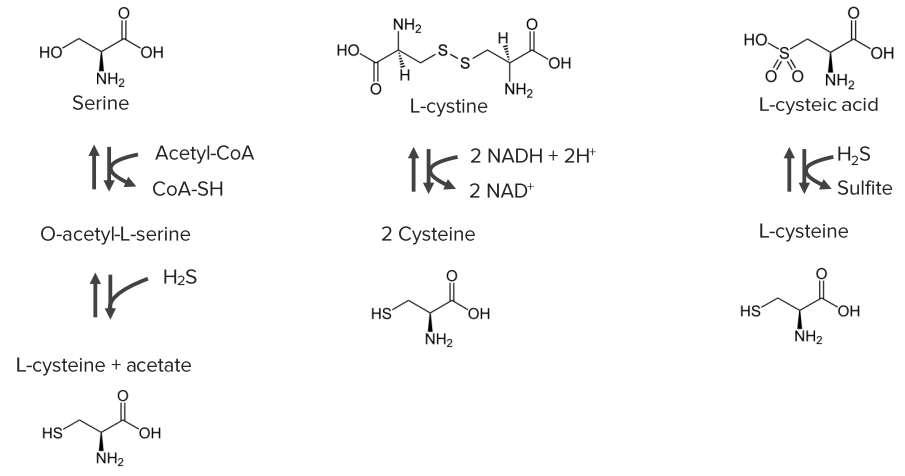
Селеноцистеиновый обмен
- Иногда называют 21-й аминокислотой
- Не указано прямо в генетическом коде
- Использует стоп-кодон с необычной структурой
- Синтезирован из серина на тРНК

Семья Аспартат
- Все члены семьи возникают из аспартата
- Аспартат можно сделать из одного из них - аспарагина
- Многочисленные дорожки ведут к аспартату
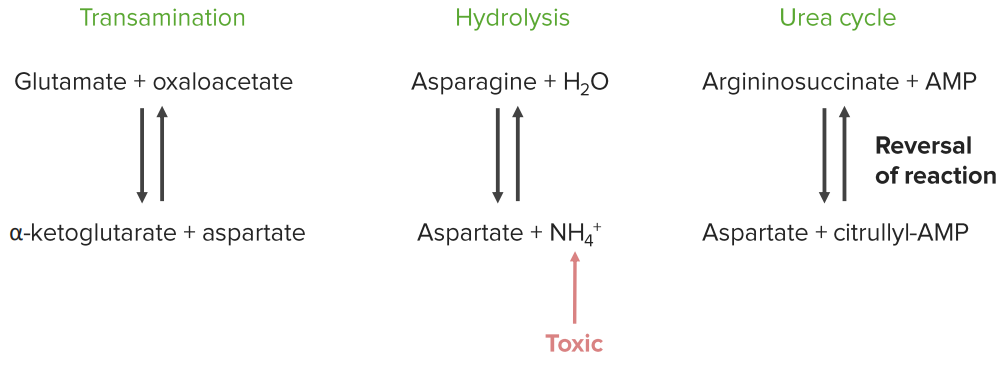
Метаболизм аспарагина
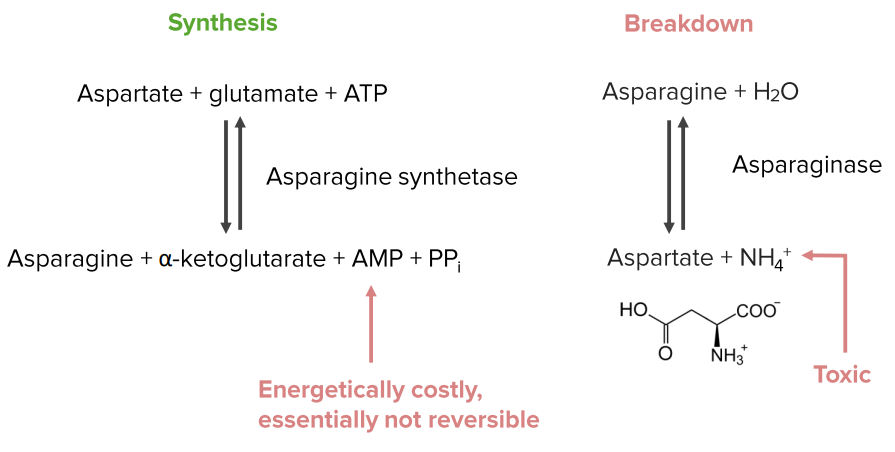
Метиониновый обмен
- Расстройство перекрывается с метаболизмом цистеина
- Сложный синтез из аспартата
Шаги к процессу
- фосфорилирования
- Окисление и дефосфорилирование
- оксидирование
- Создает гомосерин
- Сукцинилирование
- Цистеиновая замена сукцината
- Потеря пирувата и иона аммония
- Это создает гомоцистеин
- Метилирование гомоцистеина N5-метилфолатом приводит к образованию метионина (необходим витамин B12)
Гомоцистеин может быть превращен в метионин альтернативным путем справа.
- Метионин, модифицированный бактериями для использования в переводе
- Происходит после метионина на тРНК инициатора
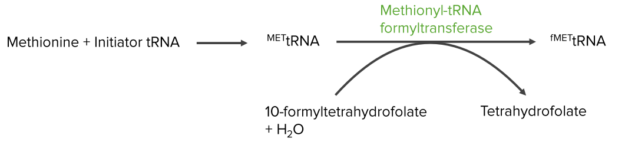
Первые три шага такие же, как метаболизм метионина, создавая гомосерин
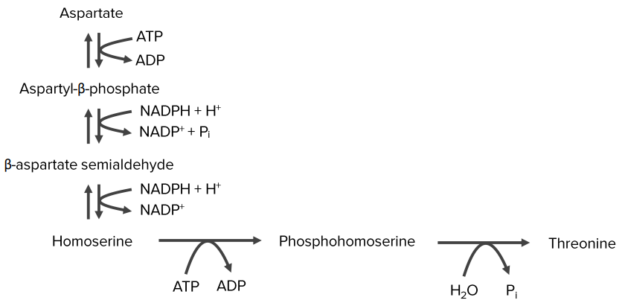
Метаболизм лизина
- Первые две реакции такие же, как у треонина и метионина
- Всего девять шагов
- Лизин является одной из наиболее пост-трансляционно модифицированных аминокислот, особенно в гистонах.
- Гидроксилирование лизина важно для получения сильного коллагена
- Дефицит одного из ферментов в пути расщепления лизина, α-аминоадипической полуальдегидсинтазы, приводит к гиперлизинемии - накоплению лизина в крови
Ароматическая Семья
Триптофан
- Интересная регуляция синтеза у бактерий
- Затухание - все 5 генов на одном опероне
- При высоком уровне триптофана транскрипция оперона прерывается на ранней стадии.
- Когда уровень триптофана низкий, транскрипция оперона продолжается через все гены
Молекулы из триптофана
Фенилаланин (PHE)
- Незаменимая аминокислота и предшественник тирозина
- PHE гидроксилаза катализирует образование тирозина из PHE
- Дефицит фермента PHE гидроксилазы вызывает фенилкетонурию
- Высокие уровни PHE вызывают повреждение мозга
- Лечится путем снижения уровня PHE
- Nutrasweet содержит PHE
Тирозин (TYR)
- Не обязательно, если присутствует PHE
- Предшественник катехоламинов - L-допа, L-дофамин, норэпинефрин и адреналин
- Пожертвует электроны для восстановления хлорофилла в фотосистеме II
- Образует радикал в рибонуклеотидредуктазе
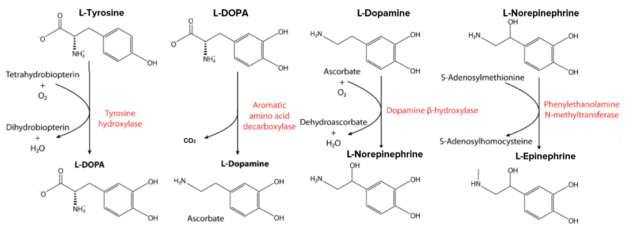
Тирозиновый обмен
Тирозин является предшественником гормонов щитовидной железы:
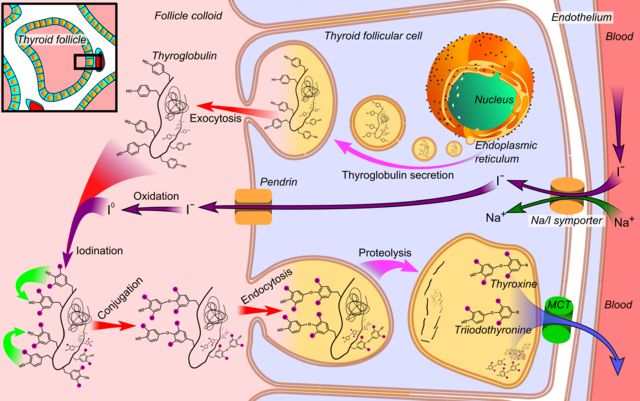
Образ : «Синтез гормонов щитовидной железы», Хэгстрем, Микаэль (2014). «Медицинская галерея Mikael Häggström 2014». ВикиЖурнал по медицине. Лицензия: СС0
Метаболизм и болезнь тирозина
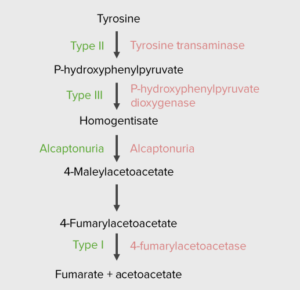 Тирозинемия - проблемы с катаболизмом тирозина
Тирозинемия - проблемы с катаболизмом тирозина
- Тип I
- Тип II
- Тип III
- Алькаптонурия - болезнь черной мочи
Лечение
- Ограниченная диета TYR / PHE
- Пересадка печени
Семья Пируват
Аланин метаболизм
- Легче всего получается из пирувата - переаминирование
- Побочный продукт катаболизма валина, лейцина и изолейцина
- Глюкозо-аланиновый цикл
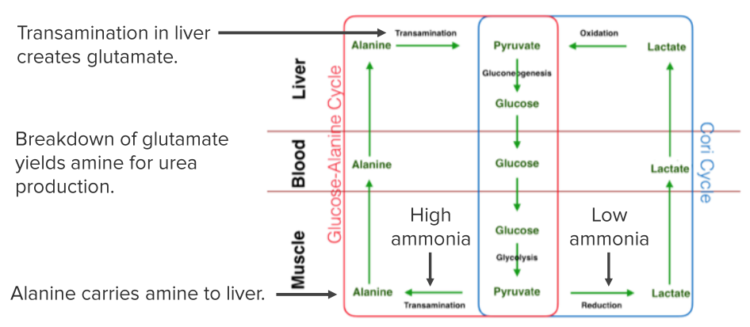
Глюкоза-аланин-цикл - важен для удаления аммиака
Метаболизм лейцина (LEU) / валина (VAL) / изолейцина (ILE)
- Аминокислоты с разветвленной цепью (BCAA)
- Несколько общих шагов
- Начать с декарбоксилирования и присоединения двух углеродного куска к ТЭС
- Пути валина и лейцина включают прикрепление двух углеродных фрагментов к пирувату
- Путь изолейцина включает присоединение двух углеродных фрагментов к α-кетобутирату
- Предпоследние продукты - α-кетоизокапроат (LEU), α-кетоизовалерат (VAL) и α-кето-β-метилвалерат (ILE) каждый трансаминируется с образованием конечной аминокислоты
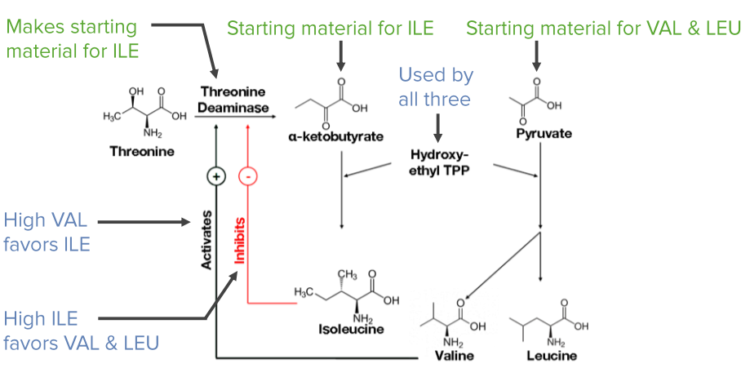
Обратная связь синтеза регулируется с помощью треонин-деаминазы
- Расщепление BCAA происходит через α-кетокислотный дегидрогеназный комплекс с разветвленной цепью
- Мутации, изменяющие этот комплекс, могут привести к болезни мочи кленового сиропа
Гистидин (HIS) метаболизм
- Самый сложный из всех аминокислот
- Перекрывает метаболизм нуклеотидов с рибозо-5-фосфатом и PRPP
- 10 шагов в пути
- Обратная связь по второму ферменту пути (АТФ-фосфорибозилтрансфераза) ингибируется гистидином
Относительно распространенным генетическим нарушением обмена веществ является фенилкетонурия, ФКУ (поражено примерно 1 на 10000 новорожденных). Каждый новорожденный тестируется на ФКУ (например, с помощью теста Гатри ), потому что большинство последствий заболевания можно избежать, соблюдая строгую диету.
Из-за дефекта фермента фенилаланин гидроксилазы аминокислота фенилаланин накапливается в ткани. Вместо этого организм превращает фенилаланин в фенилпируват кетокислоты. Этот продукт частично выделяется, что объясняет название фенилкетонурия, но частично метаболизируется, образуя цитотоксические субстраты. Они вызывают повреждения, особенно в миелиновых оболочках ЦНС. Это ухудшает нормальное развитие мозга. В основном этому способствуют избыточные количества фенилаланина по сравнению с концентрацией других аминокислот, транспортируемых через гематоэнцефалический барьер, что приводит к дефициту необходимых метаболитов. Следствием этого заболевания является умственная отсталость. Целью скрининга новорожденных является выявление пострадавших и предоставление им специальной диеты с низким содержанием фенилаланина и богатой тирозином (тирозин становится незаменимой аминокислотой для больного). Таким образом, повреждения могут быть предотвращены или, по крайней мере, предотвращены.
Другим генетически связанным заболеванием катаболизма фенилаланина является алкаптонурия, вызванная дефектным ферментом, известным как гомогентизатоксигеназы . Это менее опасно для ФКУ, у этого состояния меньше симптомов, хотя большое количество гомогентизата выводится с мочой, и лабораторные исследования подтверждают его наличие, когда образец мочи становится черным после окисления. Пациенты с алкаптонурией также склонны к развитию формы артрита.
Обзорные вопросы
Решения можно найти под ссылками.
1. Какое утверждение о аминотрансферазах неверно?
- Аминотрансферазы переносят аминогруппы между аминокислотами и альфа-кетокислотами.
- Во время реакции аминогруппа аминокислоты переводится в пиридоксальфосфат.
- Аспартатаминотрансфераза (GOT) использует альфа-кетопропионовую кислоту в качестве альфа-кетокислоты.
- Аланинаминотрансфераза (GPT) использует альфа-кетоглутаровую кислоту в качестве альфа-кетокислоты.
- При фенилкетонурии аминокислота фенилаланин все чаще трансаминируется в фенилпируват.
2. Гистамин, медиатор реакций гиперчувствительности, ферментативно образуется из гистидина в результате…
- ... декарбоксилирование.
- ... дезаминирование.
- ... гидроксилирование.
- ... метилирования.
- ... переаминирования.
3. Аммиак токсичен для организма человека, особенно для мозга. Поэтому важно предотвратить высокую концентрацию аммиака. Прямая фиксация молекулярного аммиака с ковалентной связью на молекуле субстрата может быть катализирована ...
- … Аланинаминотрансфераза.
- … Аспартатаминотрансфераза.
- ... глутаматдегидрогеназа.
- ... glutaminase.
- ... трансглютаминаза.
Похожие
МОРСКАЯ-маска и трубкаПодводное плавание - самая простая форма активного наблюдения за подводной жизнью. Аквалангист с маской, трубкой и ластами плавает по поверхности воды с погруженным лицом, наблюдая за тем, что происходит под ним. Подводное плавание культивирует тысячи людей, даже с минимальными навыками плавания. Конечно, чем больше навык, тем больше удовольствия. Самая продвинутая форма погружения в ластах - фридайвинг - Как похудеть быстро: 3 простых шага, основанных на науке
Есть много способов потерять много веса быстро. Однако большинство из них сделает вас голодным и неудовлетворенным. Если у вас нет железной силы воли, то голод заставит вас быстро отказаться от этих планов. План, изложенный здесь, будет: Значительно снизить аппетит Заставить вас похудеть быстро, без голода. Улучшите ваше метаболическое Фехтование, как раньше называлось боксом, - мой любимый вид спорта, которым я занимаюсь уже 8-9 лет....
Фехтование, как раньше называлось боксом, - мой любимый вид спорта, которым я занимаюсь уже 8-9 лет. Это долгое время, чтобы узнать что-то изнутри. Эта статья будет посвящена предоставлению вам преимуществ обучения этому благородному спортивному бою. Конечно, вы ни разу не видели этого по телевизору, или, возможно, у вас была возможность тренироваться, как бороться в таких видах спорта, как ММА, муай тай и кикбоксинг. Разница между этими видами спорта и боксом значительна. Другие боевые Ручной велосипед | Настоящий спорт, спорт для всех
... ии есть еще один Джиро д'Италия, еще одна розовая майка, еще одна группа чемпионов и энтузиастов, ожидающих следующую гонку. Это Giro d'Italia Handbike (GIHB) , первое издание которого состоялось в 2010 году благодаря идее Андреа Леони, бывшего директора рекламного каравана профессионалов Giro d'Italia. Мы попросили его поговорить с нами об этом проекте, о его социальной ценности, которая ничем не отнимает у конкурентов, и о постоянной попытке преодолеть его ограничения. Знаки безопасности на производстве
Знаки безопасности является одной из разновидностей средств коллективной защиты сотрудников, которые предназначены для профилактики воздействия опасных производственных факторов и возникновения аварий. Основной целью применения знаков безопасности является информирование сотрудников о порядке эксплуатации оборудования и дозволенного поведения в промышленных помещениях. лица, 5 лучших добавок для силы
Ты тренируешься в спортзале некоторое время и видишь, что твоя сила снижается? Так как в начале недели с недели вы смогли увеличить вес на 5-10% больше, то теперь вы чувствуете, что стоите и даже возвращаетесь? Ну, будучи новичком, имеет свои преимущества и недостатки. Преимущество в том, что ваши мышцы свежи и быстро адаптируются к условиям, которые вы создаете. Вы регенерируете быстрее и быстрее реагируете на новые стимулы, например, в виде увеличения веса, но со временем вам будет сложнее Как заработать на своем сайте, сотрудничая со Skyscanner?
Получите вдохновение от своих читателей и получите комиссию от Skyscanner! Прочтите эту статью, чтобы узнать, как заработать на публикации интересных статей и уникальных фотографий. Цель сайта - не только предоставлять контент, но и приносить реальный доход. В конце концов, кто сказал, что вы не можете иметь оба? Почему Skyscanner ищет партнеров? Все началось, когда Гарет Уильямс, студент Манчестерского университета, решил навестить своего брата во Франции. Он Термины йоги, которые вы должны знать
Так же, как артисты балета должны выучить несколько слов по-французски, а бегуны должны уметь слышать и говорить по-шведски слово fartlek, не хихикая слишком сильно, люди, которые практикуют йогу, сделают все возможное, если они смогут понять санскрит и другие термины, которые распространено в занятиях йогой и видео йоги. Если вы пожилой человек в йоге, я хотел бы услышать, какие термины вас сначала Различия между женщинами из деревень и городов
... ись ли вы, как мужчины ищут пожизненную леди? Оказывается, речь идет не только о внешности или характере. Иногда происхождение женщины также является важным фактором. Если вы родились и выросли в маленьком городе, или, возможно, вы всегда жили в большом городе - это может что-то значить для них. Смотрите также: Этот вопрос парень может задать тебе на первом свидании. От ответа Мы проверили Nintendo 2DS XL и игры: Miitopia, Hey Pikmin и другие
У меня уже была возможность сыграть в четыре совершенно новые игры, только что анонсированные Nintendo 2DS XL. Я на практике проверил, как выглядит новая портативная портативная консоль, и я думаю, что знаю, почему японцы предлагают этот продукт в контексте коммутатора. Nintendo снова вызывает эмоции у игроков. Введен в продажу в начале Switch - необычная и просто блестящая консоль но это
Комментарии
Книга отвечает на такие вопросы, как: «Каково быть влюбленным?Книга отвечает на такие вопросы, как: «Каково быть влюбленным?» Или «Что значит любить?». В качестве типичного примера в книге представлена смешанная расовая пара - с белой женщиной и мужчиной арабской внешности, которая просматривает следующие страницы, чтобы помочь детям понять, «как сделать детей». Стоит спросить себя, почему мигранты, занимающиеся сексом с белыми женщинами, всегда сталкиваются с подобными учебниками? Мы никогда не найдем там женщину с платком, встречающую белого Каковы другие побочные эффекты стероидов?
Каковы другие побочные эффекты стероидов? Чтобы преуспеть в создании тела с большими, хорошо сформированными мышцами, некоторые люди используют анаболические стероиды, синтетическую версию мужского гормона тестостерона. Анаболические стероиды - это наркотики с очень опасными побочными эффектами: нервозность, непереносимость, параноидальное чувство, частые перепады настроения, депрессия, мания, что тело нуждается в тренировках, гнев и насилие.
1. Какое утверждение о аминотрансферазах неверно?
Так как в начале недели с недели вы смогли увеличить вес на 5-10% больше, то теперь вы чувствуете, что стоите и даже возвращаетесь?
В конце концов, кто сказал, что вы не можете иметь оба?
Почему Skyscanner ищет партнеров?
Ись ли вы, как мужчины ищут пожизненную леди?
Книга отвечает на такие вопросы, как: «Каково быть влюбленным?
» Или «Что значит любить?
Стоит спросить себя, почему мигранты, занимающиеся сексом с белыми женщинами, всегда сталкиваются с подобными учебниками?
Каковы другие побочные эффекты стероидов?
